Featured Scientist

Wei-Chi Ku, Ph.D.
Associate Professor
長期使用Cabozantinib改變腎細胞癌之細胞黏附訊息傳遞並促進細胞遷移
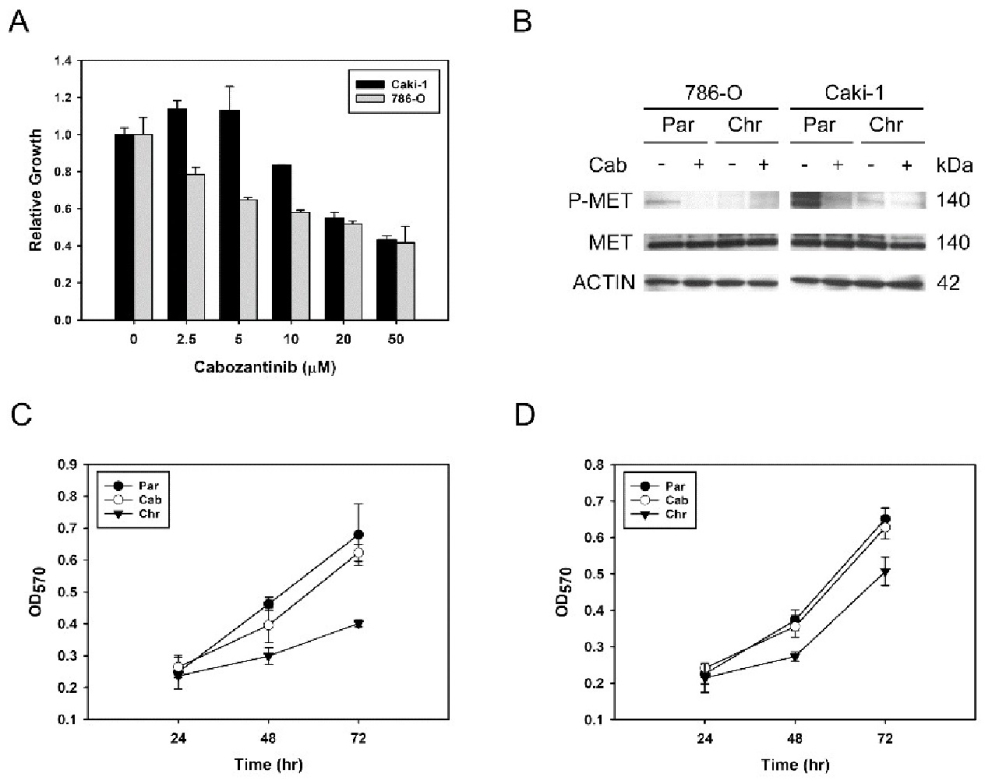
傳統標靶血管內皮生長因子受體(VEGFR)的酪胺酸激酶抑制劑(TKIs),如舒尼替尼(sunitinib),雖初期具治療效果,但最終常導致腎細胞癌(renal cell carcinoma, RCC)產生對藥物具抗性的克隆株。Cabozantinib 為新一代多重標靶 TKI,可同時抑制 VEGFR、MET 及 AXL,已被證實能改善臨床治療成果。然而,長期暴露於 cabozantinib 是否會重塑細胞內訊息傳遞網絡,進而促進適應性抗藥性,仍未釐清。本研究以 RCC 細胞為模型,長期培養於 5 μM cabozantinib 超過四個月,建立慢性暴露細胞株(Chronically treated, Chr);另以急性處理48小時之細胞作為對照組。研究設計涵蓋細胞增生與遷移能力分析,並結合二甲基標定、磷酸胜肽富集與高解析 LC-MS/MS,進行定量磷酸化蛋白質體分析。差異性磷酸化位點進一步經由 Perseus、ShinyGO、PTM-SEA 與 Cytoscape 進行功能分析。
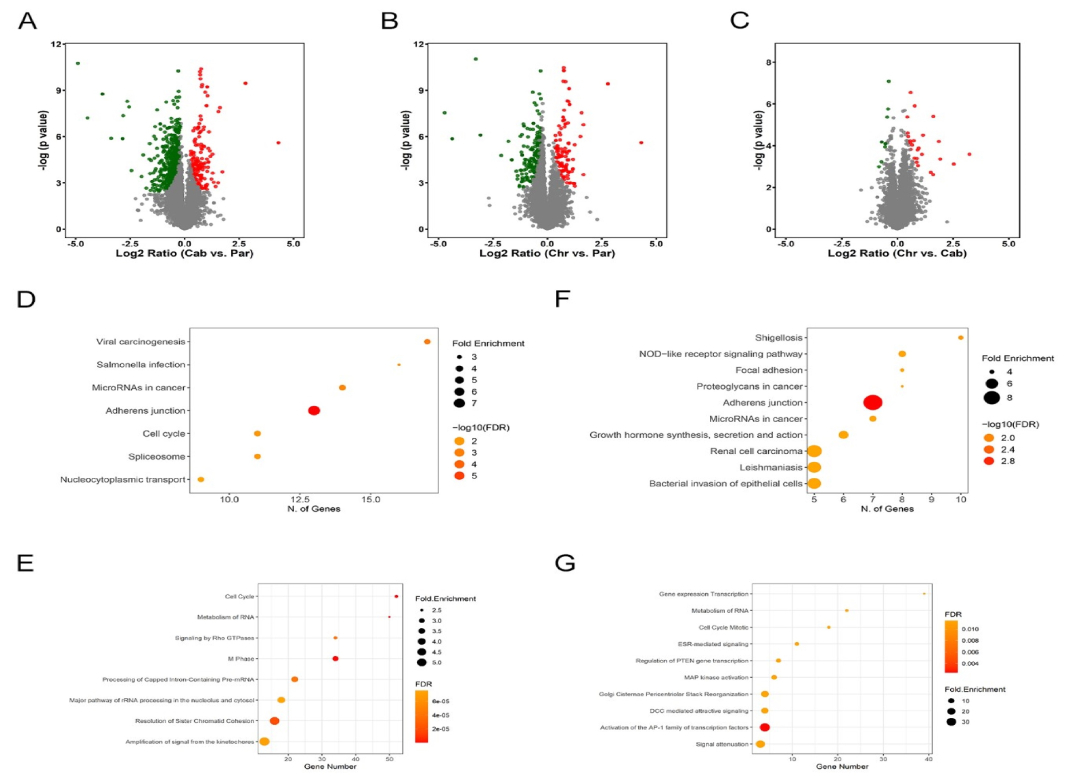
研究結果顯示,cabozantinib 急性處理可迅速抑制 MET-Y1234/1235 磷酸化、下調細胞週期激酶活性,並顯著抑制細胞增生。雖然 Chr 細胞仍維持生長停滯,但其細胞遷移與侵襲能力卻相較親代株提升近兩倍。經由磷酸化蛋白質體實驗,從Chr 細胞中共鑑定出283個顯著變動的磷酸化位點,生物資訊分析顯示與細胞貼附、PI3K–Akt–mTOR 與 MAPK/AP-1 訊息模組相關的訊號路徑被重新活化,而細胞週期調控路徑則持續下調。綜合而言,長期 Cabozantinib 處理會誘導 RCC 細胞產生一種「增殖受抑但遷移活性提升」的適應性表型,此轉變伴隨細胞貼附與 MAPK 路徑之重編程,可作為預測 cabozantinib 抗藥性與轉移風險的潛在生物標誌,並為後續聯合治療策略提供依據。
Keywords:cabozantinib, renal cell carcinoma, phosphoproteomics, tyrosine kinase inhibitor, cell migration
6 views